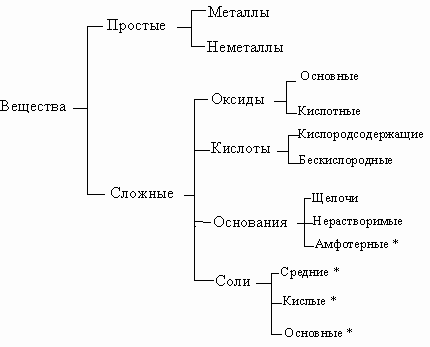
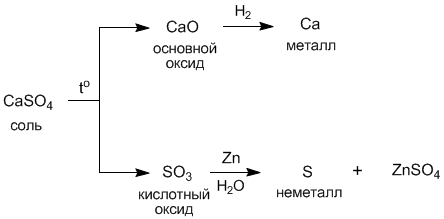
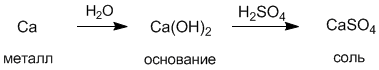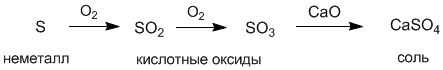Наиболее распространенные реакции солей –
реакции обмена
и реакции замещения.
1. Реакции замещения солей.
Поскольку соли состоят из ионов металла и
кислотного остатка, их окислительно-восстановительные реакции условно можно
разбить на две группы: реакции за счет иона металла и реакции за счет
кислотного остатка, если в этом кислотном остатке какой-либо атом способен
менять степень окисления.
а) Реакции за счет иона металла.
Поскольку в солях содержится ион металла в
положительной степени окисления, они могут участвовать в
окислительно-восстановительных реакциях, где ион металла играет роль
окислителя. Восстановителем чаще всего служит какой-нибудь другой (более
активный) металл. Приведем пример:
HgSO4
|
+
|
Sn0
|
=
|
Hg0
|
+
|
SnSO4
|
соль менее
активного металла (окислитель)
|
|
более
активный металл (восстановитель)
|
|
|
|
|
Принято говорить, что более активные
металлы способны вытеснять другие металлы из их солей. Металлы,
находящиеся в ряду активности леве, являются более активными.
(смотри ряд Н.Н. Бекетова)
2. Обменные
реакции солей.
Такие реакции могут происходить в
растворах, когда соли реагируют: а) с кислотами, б) с щелочами, в) с другими
солями. Например:
а) CuSO4 + H2S = CuS↓
(осадок) + H2SO4
AgNO3 + HCl = AgCl↓ (осадок) +
HNO3
б) FeCl3 + 3 NaOH = Fe(OH)3↓
(осадок) + 3 NaCl
CuSO4 + 2 KOH = Cu(OH)2↓
(осадок) + K2SO4
в) BaCl2 + K2SO4
= BaSO4↓ (осадок) + 2
KCl
CaCl2 + Na2CO3
= CaCO3↓ (осадок) + 2 NaCl
Во всех случаях один из продуктов обменной реакции обязательно
должен покидать реакционную смесь в виде осадка или газообразного вещества.
Либо должно получаться прочное соединение, не распадающееся в растворе на ионы
(например, вода в реакции нейтрализации). Если эти условия не выполняется, то
при смешивании реагентов в лучшем случае образуется смесь не реагирующих между
собой ионов - реакция не идет.
Задачи
Продолжите уравнения реакций и уравняйте их.
Если есть продукты, выпадающие в осадок или выделяющиеся в виде газа, поставьте
после них стрелку вниз или вверх.
1) AgNO3 + FeCl3 =
2) Pb(NO3)2
+ K2S =
3) Ba(NO3)2
+ Al2(SO4)3 =
4) CaCl2
+ Na3PO4 =
5) Na2S
+ HCl =
6) K2CO3
+ H2SO4 =
7) SiO2
+ NaOH =
8) NaHCO3
+ HCl =
9) MgO +
HBr =
10) MgO +
SO3 =
11)
Mg(OH)2 + H2SO4 = основная соль + ...
12) FeSO4 + KMnO4 + ... = MnSO4 +
...
А. В. Мануйлов, В. И. Родионов Основы
химии. Интернет-учебник.